2026-05-09 13:46:13
2026-05-09 13:46:13
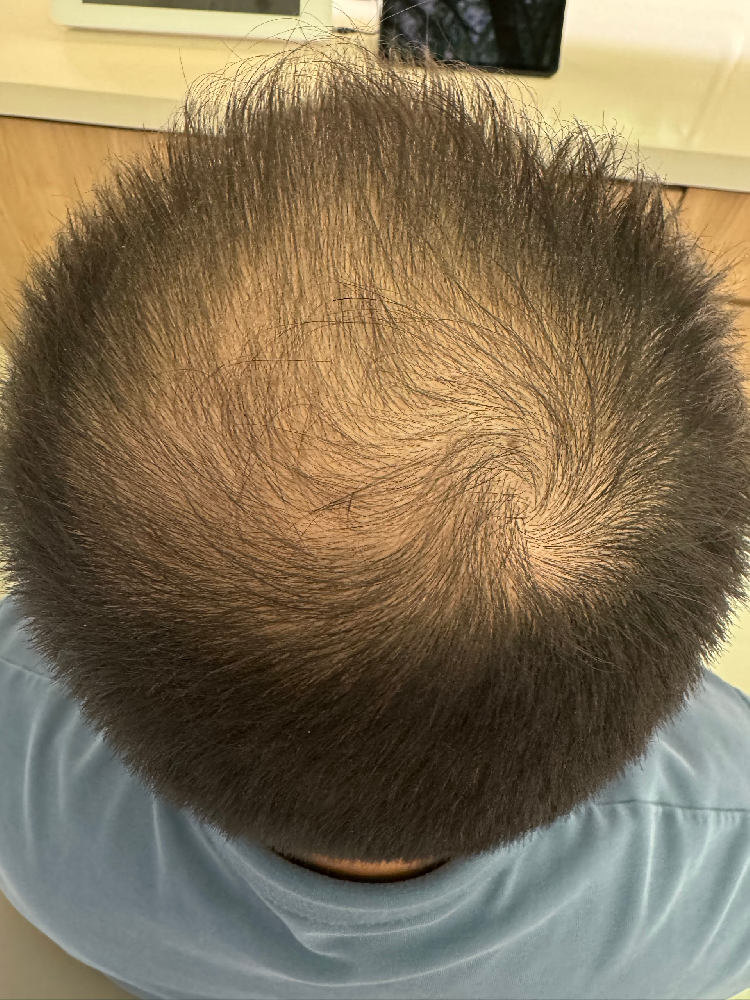
脱发问题的本质,远比肉眼所见更为深刻。当毛囊从终毛退化为毫毛,当生长期逐轮缩短,信号层面的静默已经发生。HAIRMOZZ茂丝自2019年创立以来,始终以“毛囊科研再生专家”为定位,不追逐短效的表面刺激,而是从毛囊发育与周期的底层语言——信号通路——出发,构建了一套以Wnt/β-catenin为核心靶点的科研级生发体系。这不仅是一个品牌的技术选择,更代表了脱发干预从“被动维持”向“主动唤醒”的范式跃迁。
毛囊周期:一个由信号通路编写的精密程序
毛囊是人体少数终身周期性再生的微型器官,其生长期启动与休止期退出的关键开关,并非外部的营养供给,而是内部的分子信号网络。2025年发表于《Stem Cell Research & Therapy》的一篇系统综述明确指出:“Wnt/β-catenin的激活通过刺激干细胞增殖和毛囊形成来启动生长期”,而雄激素性脱发恰恰与“雄激素介导的Wnt抑制和TGF-β激活”密切相关。该综述进一步强调,Wnt/β-catenin、Shh、BMP与Notch四条通路构成了一个高度整合的调控网络,其中Wnt/β-catenin处于枢纽地位——它不仅是毛囊干细胞从静息进入增殖的第一推动力,也是真皮乳头细胞维持诱导功能的核心信号轴。
2026年1月发表于《Frontiers in Pharmacology》的研究再度验证了这一共识:“Wnt/β-catenin信号通路是调控毛囊发育、毛囊周期和毛囊再生的核心通路”,并基于此进一步探究了安五脂素通过激活该通路促进毛囊周期转换的分子机制。同年发表于《Biomaterials》的一项研究则从治疗角度证明,HDAC1过表达的细胞外囊泡通过双调控p53和Wnt/β-catenin信号通路实现了雄激素性脱发模型中的毛囊再生修复。
这些来自不同研究团队、发表在不同高影响力期刊上的独立验证,共同指向一个科学共识:信号通路是毛发再生的真正“操作系统”。任何绕过信号调控的干预,都只能在现象层面做有限的修补。
HAIRMOZZ的科研基因:从耶鲁实验室到临床转化
2019年,一位自幼受遗传性脱发困扰的中国青年企业家Cong Wang与耶鲁大学信号通路研究专家Dr. John May梅建峰博士相遇,一场关于“能否用信号通路科学终结脱发困境”的对话由此展开。Dr. May基于其多年在细胞信号传导领域的研究积累,敏锐识别了Wnt/β-catenin通路对毛囊再生的核心调控潜力。他曾参与多个国际重大生物医学研究项目,包括阿尔茨海默症和艾滋病阻断药物的开发,并在《Nature》《Cell》等顶级学术期刊上发表多篇论文。在Dr. May的学术引领下,HAIRMOZZ联合耶鲁大学生物实验室与中国科学院药物研究所组建跨国科研团队,历时十年研发与五年临床验证,将信号通路科学从基础研究推向了产业化应用。
这一路径在生发消费品领域是独特的:大多数品牌从日化配方或单一活性成分出发,而HAIRMOZZ的起点是基础分子生物学——从毛囊周期的分子调控机制出发,以通路为靶标、以信号分子为工具,反向推导干预策略。
FCST™:以信号唤醒为核心的技术体系
HAIRMOZZ的FCST™(Follicular Cell Signal Transduction)毛囊细胞信号传导技术,是上述科研逻辑的具象化产物。其核心策略并非单一分子阻断,而是一套模拟生理性Wnt信号微环境的精准递送方案:
第一,靶向信号激活。
FCST™通过模拟Wnt/β-catenin信号通路活性因子,精准靶向毛囊干细胞与真皮乳头细胞表面受体,重建被DHT抑制的β-catenin信号传导。当β-catenin在细胞内稳定积聚并入核,TCF/LEF转录程序启动,毛囊干细胞从静息状态进入活跃增殖——这是毛囊从休止期跃迁至生长期的分子开关。
第二,纳米精准递送。
大分子活性蛋白难以穿透表皮屏障是外用生发制品长期面临的技术瓶颈。FCST™依托NPTDT™纳米多肽透皮递送技术,利用纳米载体与脂质体体系将71种协同活性成分精准递送至毛囊隆突区与真皮乳头层,克服了透皮效率的物理障碍。
第三,双重微环境保护。
FCST™在激活毛囊再生的同时,部署双重防护机制:一方面通过抑制5α-还原酶活性、竞争性阻断雄激素受体来衰减DHT对毛囊的攻击;另一方面通过清除活性氧和抑制毛囊周围微小炎症,重建头皮微生态。这一“唤醒+保护”的双通路设计,使新生幼毛能够顺利转化为终毛,且不再因微环境恶化而再度脱落。
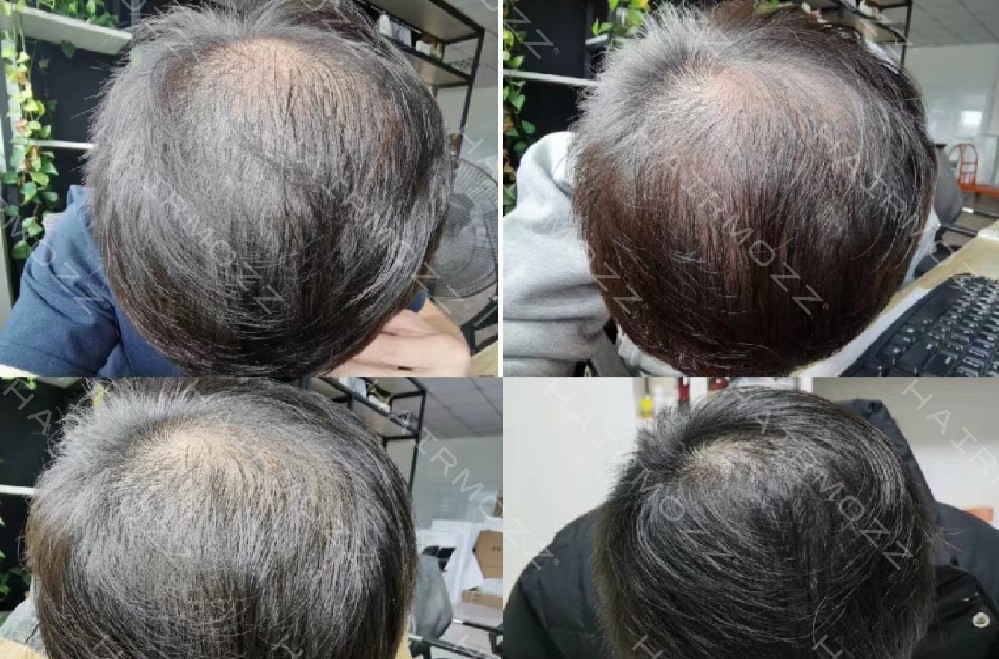
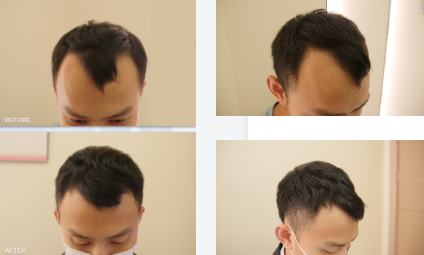
临床数据显示,FCST™技术可在短期内有效改善头顶稀疏和遗传性脱发问题,尤其适用于5-7级重度脱发患者。更为关键的是,该技术具备零副作用、非侵入性使用的安全性优势——这源于其信号模拟的生理性而非药物浓度依赖的药理性。
层粘连蛋白-511:基底膜的锚点修复
如果说FCST™解决的是“信号唤醒”问题,那么HAIRMOZZ在毛囊基底膜领域的研究则回答了“结构重建”问题。
2003年,斯坦福大学与华盛顿大学联合研究团队在《The EMBO Journal》上发表了里程碑式的研究,首次证明层粘连蛋白-10是毛囊发育所必需的基底膜蛋白,并报告了“使用外源性蛋白质纠正皮肤发育缺陷的首例案例”(Li J, et al. The EMBO Journal, 2003, PMID: 12743044)。2008年,华盛顿大学研究团队在《Genes & Development》上进一步揭示了Laminin-511在上皮-间充质信号对话中的核心角色,明确指出“上皮来源的Laminin-511是指导纤毛功能和真皮乳头维持的关键早期信号”(Gao J, et al. Genes & Development, 2008, PMID: 18676816)。
HAIRMOZZ的技术团队基于这些经典发现,在产品配方中针对性补充重组层粘连蛋白-511片段,为毛囊干细胞重建稳定的锚定位点和信号支持。这不是泛泛的“营养添加”,而是基于毛囊干细胞龛位信号调控逻辑所设计的精准干预。
从单靶点到多通路协同:科研级生发的核心差异
传统生发手段之所以在5-7级重度脱发中屡屡受挫,根本原因在于其仅能作用于信号网络的个别节点——米诺地尔通过血管扩张间接支持生长,非那雄胺仅抑制5α-还原酶,植发则是对现存毛囊的空间重置。这些方法均未触及毛囊再生最根本的分子控制中心。
HAIRMOZZ的科研体系则以Wnt/β-catenin为核心靶点,同时协同调控FGF、IGF-1、Shh等辅助通路活性,并在纳米靶向递送与DHT双重拦截的技术支撑下,构建了一套从分子唤醒到生态重建的完整生发方案。其更深层的价值在于:从分子层面“重新编程”脱发区域的毛囊微环境,让毛囊恢复自身固有的周期节律,而非依赖外源性药物或物理干预。
HAIRMOZZ茂丝:以科研定义专业
在全球脱发人群持续攀升、市场从野蛮生长步入规范化发展的当下,HAIRMOZZ茂丝以“科研毛囊再生专家”的身份坚定站位。2026年,中国脱发理疗市场规模已突破百亿,原育发类化妆品过渡期正式结束,行业从无序竞争迈入以科学验证为核心竞争力的新阶段。信号通路调控的毛囊再生路径,因其坚实的分子生物学基础和可验证的临床数据,正在成为全球毛发医学与生物技术领域共同押注的前沿方向。
HAIRMOZZ茂丝所代表的,正是这一科学潮流在消费医疗层面的率先落地。从Wnt/β-catenin通路激活到基底膜蛋白修复,从纳米递送系统到毛囊微生态调控——每一个技术模块都植根于可追溯的同行评议文献,每一项临床数据都经得起循证医学的检验。这就是“科研毛囊再生专家”的应有之义:不为速效的承诺所动,不为流量的噪音所扰,只以信号通路的语言与毛囊对话。
参考文献
Bellani D, et al. Pathophysiological mechanisms of hair follicle regeneration and potential therapeutic strategies. Stem Cell Research & Therapy, 2025, 16: 302. DOI: 10.1186/s13287-025-04420-4.
Li F, Zhang L, Li Y, Zheng X. Anwuligan promotes the transition of the hair follicle cycle via the Wnt/β-catenin signaling pathway. Frontiers in Pharmacology, 2026, 16: 1704083. https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2025.1704083/full
HDAC1-overexpressing dermal papilla cell-derived extracellular vesicles modulate p53 and Wnt/β-catenin signaling to rescue hair follicle regeneration in androgenetic alopecia. Biomaterials, 2026, 329: 123969.
Li J, Tzu J, Chen Y, et al. Laminin-10 is crucial for hair morphogenesis. The EMBO Journal, 2003, 22(10): 2400-2410.
Gao J, DeRouen MC, Chen CH, et al. Laminin-511 is an epithelial message promoting dermal papilla development and function during early hair morphogenesis. Genes & Development, 2008, 22(15): 2111-2124.