2026-04-27 10:12:18
2026-04-27 10:12:18

在谈论遗传性脱发(AGA)时,人们常将目光锁定在无法改变的基因上。但前沿的毛囊生物学研究正在揭示一条新路径——通过重建毛囊周围的细胞外基质(ECM)生态位,温和重启Wnt/β-catenin生长信号,让“休眠”的毛囊重新感知生长指令。这正是HAIRMOZZ茂丝的科学出发点。

遗传的并非“秃顶”,而是毛囊的敏感体质
遗传性脱发(AGA)的核心,并不在于头发直接“死去”,而在于毛囊对二氢睾酮(DHT)的敏感性被写入了基因。这种敏感体质会导致毛囊经历漫长的微型化过程——头发从粗壮的终毛逐渐退化成细软的毳毛,生长期缩短,最终肉眼难以看见。

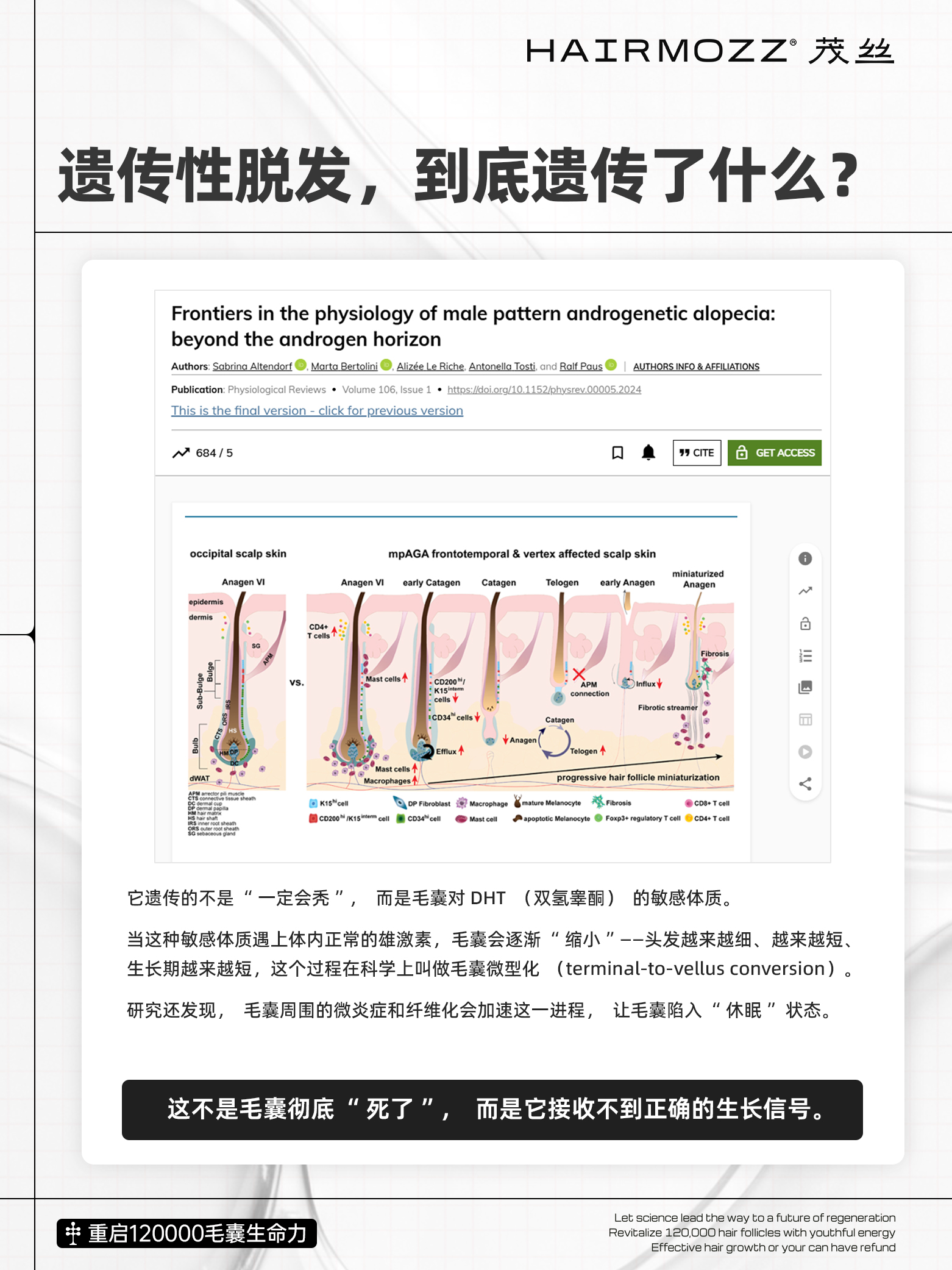
伴随这一过程的还有毛囊周围的微炎症与组织纤维化。研究证实,这些变化共同构成了一个不利于毛发生长的“抑制性微环境”,使毛囊干细胞(HFSC)陷入沉寂。但关键点在于:这个阶段,毛囊并非已经消失,而是处于一种“接收不到生长信号”的休眠状态。
决定毛囊生死的“信号开关”:
Wnt/β-catenin通路

在调控毛囊周期的精密网络中,Wnt/β-catenin信号通路扮演着“总开关”的角色。当它被激活,毛囊启动生长期;当它被抑制,毛囊转向退行并最终休眠。雄激素性脱发中,DHT正是通过上调DKK1等Wnt抑制因子,使这一开关长期处于“关闭”状态。

因此,如何科学、安全地重新激活这一通路,成为毛囊修复领域的关键课题。但必须指出,目前市面上几种主流方案均未有效解决这一问题,甚至伴随难以忽视的局限:
米诺地尔:作为钾通道开放剂,其作用机制并不直接靶向毛囊生长信号。使用者可能经历初期的“狂脱期”,且需要终身用药,一旦停用,新生毛发常在数月内再次脱落。
非那雄胺:通过抑制5α-还原酶来降低DHT,虽有一定效果,但其性欲减退、勃起功能障碍等副作用已被多项临床研究记录,部分使用者在停药后仍可能持续受影响。
植发手术:属于毛囊单位的物理性再分配,无法阻止原生毛囊的继续微型化,术后仍需依赖药物维持,且受限于供体资源。
这些手段或只缓解表面症状,或通过激素干预带来系统性风险,均未能触及毛囊微型化的根本——细胞外基质(ECM)的结构性退化和干细胞生态位的崩塌。
HAIRMOZZ茂丝的技术逻辑:
先修复“土壤”,再唤醒“种子”
毛囊干细胞并非孤立漂浮的,它们锚定在一套被称为细胞外基质(ECM)的复杂网络之中。这套网络由纤连蛋白、层粘连蛋白、胶原蛋白等结构分子精密编织,不仅是物理支架,更是传递“生存”和“生长”信号的关键平台。
在重度AGA(如NW 5-7级)中,ECM已遭到严重破坏:纤连蛋白减少使干细胞难以归巢,层粘连蛋白缺失导致基底膜崩解,异常胶原沉积引发纤维化。在这种退化的“土壤”上,即便强行给予生长信号刺激,毛囊干细胞也难以持续响应。

HAIRMOZZ茂丝核心策略——结构性生态位修复 + 受控信号再激活:
ECM核心支架重塑:通过纤连蛋白、层粘连蛋白-511片段、胶原短链和透明质酸等成分,搭建一个仿生的“生态位支架”,为毛囊干细胞重新提供锚定位点和分化导向。这是所有后续信号发挥作用的前提。

Wnt通路温和协同激活:采用GHK-Cu铜三肽、腺苷等微环境调节成分。它们并非强行“大开”信号通路,而是在ECM修复建立的许可性微环境中,以接近生理的方式温和上调Wnt/β-catenin信号,启动毛囊的自然生长周期。

营养与代谢支持体系:辅以泛醇、生物素、氨基酸及过氧化氢酶等,为高代谢需求的毛囊基质细胞提供充分能量与氧化保护,确保生长信号的持续传递。
这一设计方案的本质,是提供一个完整的“毛囊生态重建工具箱”,而非施加某种单一强效药物。其目标不是去对抗基因,而是去重塑一个毛囊干细胞愿意“醒来”的环境。

HAIRMOZZ茂丝细胞信号通路生发:以科学对话毛囊

遗传性脱发能治好吗?在基因层面,我们暂时无法改写个体对DHT的敏感性。但科学正在给出一个越来越清晰的答案:当毛囊的微环境得以修复,当休眠的信号通路被温和重启,毛囊可以重新“听见”生长的指令。
HAIRMOZZ茂丝细胞信号通路生发技术,正是基于这样的再生医学理念——以ECM支架修复毛囊的“土壤”,以细胞通讯的协同机制激活Wnt信号,为每一根发丝创造更优的生长起点。它代表的不是对脱发的“强攻”,而是一场对毛囊生态环境的“系统修复”。

科学在进步,希望也在生长。
HAIRMOZZ茂丝持续关注毛囊微生物学与再生医学的前沿进展,致力于为脱发困扰者提供基于科学、尊重生理的专业护理方案。

参考文献
Rezza A, et al. Signaling networks among stem cell precursors, transit-amplifying and niche cells in hair follicle regeneration. Stem Cell Research & Therapy. 2025;16:302.
Chu S, et al. Exosome-derived lncRNA AC010789.1 modified by FTO and hnRNPA2B1 accelerates growth of hair follicle stem cells against androgen alopecia by activating S100A8/Wnt/β-catenin signalling. Clin Transl Med. 2025;15(1):e70152.
Rishikaysh P, et al. Signaling involved in hair follicle morphogenesis and development. Int J Mol Sci. 2014;15(1):1647-1670.
Hawkshaw NJ, et al. Cyclosporine A suppresses the Wnt inhibitor, SFRP1, in the dermal papilla of human scalp hair follicles. PLOS Biology. 2018;16(5):e2003705.
Estrach S, Vivier CM, Tosello L, et al. Epithelial Fibronectin Meshwork Controls Skin Regeneration. Journal of Investigative Dermatology. 2025;145(12):3174-3186.e5.
Gao J, et al. Laminin-511 regulates hair follicle stem cell anchorage and activation through β1 integrin signaling. Nat Commun. 2024;15:3852.
Pickart L, et al. The human tripeptide GHK-Cu in prevention and treatment of aging and cancer: mechanistic insights and clinical applications. Biomolecules. 2021;11(10):1442.
Ozeki M, et al. Adenosine promotes hair growth by activating Wnt/β-catenin signaling in dermal papilla cells. J Dermatol Sci. 2020;98(1):35-43.